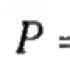Эрадикационная терапия хеликобактер пилори схема. Современные аспекты эрадикации Helicobacter pylori
Открытая в 1982-м австралийцами Б. Маршаллом и Р. Уорреном инфекция Helicobacter pylori является виновницей язвенных болезней различных участков желудка и кишечника. Для борьбы с ней международным медицинским сообществом разработаны различные схемы эрадикационной терапии.
Опасный сосед
В настоящее время не подлежит сомнению высокая степень ассоциации пептических язв с жизнедеятельностью хеликобактер пилори в слизистой желудка. Для лечения используется комплексная эрадикационная терапия - это действия, направленные на полное освобождение от инфекции, которые сводят к минимуму вероятность рецидивирования язв.
В последующие за открытием Н. pylori годы появились сообщения о том, что эта бактерия является этиологическим фактором целого ряда других заболеваний: хронического активного антрального гастрита (типа В), атрофического гастрита (типа А), некардиального рака, MALT-лимфомы, идиопатической железодефицитной анемии, идиопатической тромбоцитопенической пурпуры и анемии, обусловленной дефицитом витамина В12. Продолжается изучение взаимосвязи спиралевидной бактерии с аллергическими, респираторными и другими внежелудочными заболеваниями.
Эрадикационная терапия у детей
Необходимость эрадикации инфекции H. pylori у детей показана в многочисленных клинических исследованиях и их метаанализах, которые послужили основой для составления и регулярного обновления международного согласительного документа, хорошо известного практикующим гастроэнтерологам как Маастрихтский консенсус. В настоящее время вопросы диагностики и лечения хеликобактер-ассоциированных заболеваний регламентируются уже четвертым Маастрихтским консенсусом, принятым в 2010 году.
В развитых странах Европы, Америки и в Австралии, где с момента открытия этиологической роли Н. pylori систематически разрабатывались и внедрялись в практику методы диагностики и лечения данной инфекции, отмечен спад заболеваемости язвенной болезнью и хроническим гастритом. Кроме того, в этих государствах впервые за десятилетия наметилась тенденция к снижению заболеваемости раком желудка, чему также способствует эрадикационная терапия.

Загадочная бактерия
На основании результатов многочисленных рандомизированных плацебо и сравнительных исследований определена эффективность пробиотических средств при различных клинических ситуациях, в том числе и при хеликобактерной инфекции у детей. Однако, несмотря на некоторые достижения в понимании действия пробиотиков на бактерию H. pylori, ее тонкие механизмы остаются малоизученными.
Основным ингибирующим и бактерицидным фактором Lactobacillus является молочная кислота, которую они производят в больших количествах. Молочная кислота ингибирует активность уреазы H. pylori и, как предполагают, оказывает свое антимикробное действие за счет снижения рН в пространстве люмена желудка. Однако было установлено, что молочная кислота, которая производится клетками слизистой желудка (СОШ), способствует росту колонии H. pylori. Кроме молочной кислоты лактобактерии и некоторые другие пробиотические штаммы продуцируют антибактериальные пептиды.
Комплексная терапия
Концепция эрадикационной терапии базируется на комбинировании препаратов. ИПП (ингибиторы протонной помпы) блокируют фермент уреазу и накопление энергии внутри H. pylori, а также повышают pH на слизистой желудка, создавая условия для действия антибактериальных препаратов. Соли висмута, скапливаясь в бактерии, мешают ферментной системе патогена, позволяя иммунной системе ребенка эффективнее справляться с «вторженцем». Наконец, самой разнородной является группа антибактериальных препаратов.
Эрадикационная терапия при язвенной болезни у детей (как и при гастрите) часто предполагает использование нитроимидазолов, макролидов, лактамов, тетрациклина и нитрофуранов. Хеликобактер вырабатывает устойчивость именно к антибактериальным компонентам, что снижает эффективность эрадикационной терапии. И актуальность этой проблемы растет с каждым десятилетием.

Резистентность к антибиотикам
Выработка устойчивости к антибиотикам - общая черта, присущая всем патогенным микроорганизмам. Это эволюционный механизм, который обеспечивает их выживание в изменяющихся условиях. Резистентность Н. pylori подразделяют на:
- Первичную (следствие предшествующего лечения).
- Вторичную (приобретенная мутация микроорганизма, которую «подстегивает» эрадикационная терапия).
Причины устойчивости к лечению
В числе главных причин формирования приобретенной резистентности H. pylori ученые называют:
- Рост назначений антибактериальных препаратов этих же групп по другим показаниям.
- Бесконтрольное самолечение антибиотиками в странах, где они продаются без рецепта.
- Неадекватно назначенная эрадикационная терапия гастрита или язвы (назначение низких доз антибиотиков, сокращение курсов лечения, неправильная комбинация в схеме препаратов).
- Несоблюдение предписаний врача пациентами.
- Появление на фармацевтических рынках препаратов низкого качества.
В результате всего перечисленного рост резистентности H. pylori сокращает и без того ограниченное количество антибиотиков, активных в отношении данного микроорганизма.
Проблема антибиотикорезистентности особенно актуальна для детей, которым показана эрадикационная терапия язвенной болезни. Чаще всего они инфицируются первично резистентными микроорганизмами от родителей и близких родственников.
Кроме того, в детской популяции особенно распространено необоснованное применение антибиотиков для лечения других заболеваний, чаще всего респираторных инфекций, что также способствует селекции первично устойчивых штаммов. Нарушение режима эрадикационной терапии, как и у взрослых, приводит к формированию вторичной резистентности. Развитие устойчивости патогенна также связано с мутациями разных генов хеликобактерии.

Диагностика
Эрадикационная терапия у подростков начинается после всеобъемлющей диагностики. Первичной целью обследования ребенка, у которого наблюдаются гастроинтестинальные симптомы, является определение причины возникновения этих симптомов, а не только наличия H. pylori. При этом проведение тестов на выявление хеликобактера не рекомендуется у детей с функциональной абдоминальной болью. Можно рассмотреть целесообразность проведения тестов на выявление патогена:
- у пациентов, в семейном анамнезе которых есть рак желудка у родственника первой степени родства;
- при рефрактерной железодефицитной анемии (если исключены другие причины заболевания).
Не хватает достаточных практических доказательств причастности H. pylori к среднему отиту, инфекциям ВДП, пародонтиту, пищевой аллергии, синдрому внезапной детской смерти, идиопатической тромбоцитопенической пурпуре, низкому росту. Но подозрения есть.
Диагностические тесты
Эрадикационная терапия при язвенной болезни и гастрите определяется диагностическими тестами. Методика тестирования зависит от многих факторов:
- Для диагностики хеликобактера при проведении эзофагогастродуоденоскопии рекомендуется провести биопсию антрального отдела желудка для дальнейшего гистологического анализа.
- Рекомендуется, чтобы первоначальный диагноз H. pylori был основан на следующих данных: положительное гистологическое исследование и положительный тест на уреазу (как альтернатива - положительные результаты культурального исследования).
- C-уреазный дыхательный тест является надежным неинвазивным методом для определения того, состоялась ли эрадикация H. pylori.
- Иммуноферментный анализ кала также является надежным неинвазивным тестом для определения того, состоялась ли эрадикация бактерии.
- Тесты, основанные на выявлении антител к хеликобактерии в сыворотке, цельной крови, мочи и слюне, наоборот, надежными не являются.

Показания
Какие нужны показания к эрадикационной терапии:
- При наличии язвенной болезни и инфицировании хеликобактером.
- Если язвенной болезни нет, а инфекцию H. pylori выявили по результатам исследования образцов, взятых с помощью биопсии, эрадикация возбудителя необязательна, но возможна.
Эпидемиология
Определение уровня резистентности в отдельно взятой стране, регионе или популяции - сложная задача, требующая больших материальных и человеческих ресурсов. Еще сложнее сравнивать данные, полученные в разных странах из-за различий в методологии исследований. Например, по материалам длительных исследований в Европе (2003-2011 гг.), устойчивость патогена к «Кларитромицину» составляла от 2 до 64 % в разных странах. По данным российских авторов, резистентность к «Кларитромицину» варьируется от 5,3 до 39 %.
Из препаратов, которые применяются в схемах эрадикации, наименьшую устойчивость к резистентности формирует амоксициллин, а наибольшую - «Метронидазол». Продолжает расти устойчивость Н. pylori к препарату «Кларитромицин».
Проблемы использования «Метронидазола» и «Фуразолидона»
Эрадикационная терапия раньше часто проводилась вышеуказанными препаратами. Однако рост приспосабливаемости бактерий к «Метронидазолу» резко снизил эффективность схем лечения с его использованием. «Метронидазол» по этой причине во многих странах сегодня исключен из схем лечения.
Альтернативой «Метронидазолу» стали препараты нитрофуранового ряда, в частности «Фуразолидон». Эффективность эрадикации на его основе в комбинации с висмутом составляет 86 %. Однако «Фуразолидон» токсичен - в детской терапии во многих клиниках он не используется. К числу недостатков «Фуразолидона» относятся гепато-, нейро- и гематотоксичность, подавление микрофлоры, неудовлетворительные органолептические свойства. Для достижения требуемой концентрации действующего вещества в организме данный препарат приходится принимать четыре раза в день. Эти качества «Фуразолидона» значительно снижают полезное действие всей схемы лечения и, как следствие, эффективность эрадикации.

Препарат нового поколения
Многие лаборатории фармацевтических фирм разрабатывают менее токсичные, но эффективные против хеликобактера лекарства. Настоящим прорывом стал препарат «Макмирор», содержащий в качестве действующего вещества нифуратель. Современная альтернатива «Фуразолидону» разработана и синтезирована научно-исследовательской компанией Polichem (Италия). «Макмирор» обладает широким спектром антибактериального, противогрибкового и антипротозойного действия. Эрадикационная терапия для детей стала более безопасной.
Использование «Макмирора» позволяет усовершенствовать существующие схемы эрадикации хеликобактера у детей, повысить их эффективность и безопасность. «Нифуратель» включен в обновленные протоколы лечения H. pylori - ассоциированного хронического гастрита, гастродуоденита и язвенной болезни у детей.
Использование препарата «Макмирор» сопровождается высоким комплайенсом, так как благодаря двенадцатичасовому периоду полувыведения он может назначаться два раза в сутки. Применяется у детей с шестилетнего возраста, суточная доза при лечении лямблиоза и в схемах эрадикации хеликобактера - 30 мг в сутки на килограмм массы ребенка.
Схемы эрадикационной терапии
Примеры терапии первой линии. Однонедельные тройные схемы с препаратом висмута:
- Коллоидный субцитрат висмута (КСВ) дополняется «Амоксициллином» («Рокситромицином») или «Кларитромицином» («Азитромицином») плюс «Нифуратель» («Фуразолидон»).
- Во второй схеме «Нифуратель» заменяется «Фамотидином» («Ранитидином»), остальные препараты те же.
Однонедельные тройные схемы с ингибиторами протонной помпы:
- «Омепразол» («Пантопразол») дополняется амоксициллином или «Кларитромицином» плюс «Нифуратель» («Фуразолидон»).
- То же самое, но «Нифуратель» заменяется на КСВ.
В качестве лечения второй линии применяется эрадикационная терапия с четырьмя компонентами: КСВ работает вместе с «Омепразолом» («Пантопразолом»), «Амоксициллином» (или «Кларитромицином») и «Нифурателем» («Фуразолидоном»).

Дозы
Протоколами также регламентируются дозы препаратов, которые следует использовать в эрадикационных схемах у детей (ежесуточно на килограмм веса):
- КСВ - 48 мг (максимум 480 мг в сутки).
- «Кларитромицин» - 7,5 мг (максимум 500 мг).
- «Амоксициллин» - 25 мг (максимум 1 г).
- «Рокситромицин» - 10 мг (максимум 1 г).
- «Фуразолидон» - 10 мг.
- «Нифуратель» - 15 мг.
- «Омепразол» - 0,5-0,8 мг (максимум 40 мг).
- «Пантопразол» - 20-40 мг (без учета веса).
- «Ранитидин» - 2-8 мг (максимум 300 мг).
- «Фамотидин» - 1-2 мг (максимум 40 мг).
Особенности лечения
Какое лечение следует применять в той или иной ситуации:
- Детям, инфицированным H. pylori и имеющим в семейном анамнезе рак желудка у родственника первой степени родства, можно назначить эрадикационную терапию.
- Рекомендовано в разных регионах проводить надзор за распространенностью антибиотикорезистентных штаммов Helicobacter.
- В регионах/популяциях, в которых распространенность резистентности Helicobacter к «Кларитромицину» высока (> 20 %), рекомендуется перед началом тройной терапии, предусматривающей применение «Кларитромицина», определять чувствительность к этому антибиотику.
- Рекомендуемая продолжительность тройной терапии - 7-14 суток. При рассмотрении этого вопроса следует учесть расходы, приверженность к лечению и побочные эффекты.
- Для оценки результатов проведенной эрадикационной терапии рекомендуется применить надежные неинвазивные тесты спустя 4-8 недель после лечения.
Если не помогло
- Эзофагогастродуоденоскопия с последующим культивированием и определением чувствительности к антибиотикам, включая альтернативные, если это не было сделано перед лечением.
- Флуоресцентная гибридизация in situ (FISH) для определения резистентности к «Кларитромицину» с применением образцов, взятых при первой биопсии и залитых в парафин, если определение чувствительности к этому антибиотику не проводилось перед лечением.
- Модификация лечения: добавить антибиотик, назначить другой антибиотик, добавить препарат висмута и/или повысить дозу, и/или увеличить продолжительность терапии.
Вывод
Эрадикационная терапия - это действенное (порой единственное) средство борьбы с опаснейшей бактерией Helicobacter pylori, способной спровоцировать язвы, гастриты, колиты и прочие болезни ЖКТ.
Хеликобактер пилори - бактерия, способная становиться возбудителем болезней двенадцатиперстной кишки и желудка. Язвы, гастрит, дуоденит и даже раковые опухоли нередко являются следствием распространения данного микроорганизма. За счет особого строения бактерии удается внедряться в слизистую оболочку и спокойно создавать колонии там.
При лечении заболеваний, связанных с хеликобактер пилори, важно обеспечить комплекс мер по полному уничтожению бактерий. Эффективным он считается лишь в том случае, если вероятность выздоровления приближается к отметке в 80%. Среднестатистическая продолжительность такого лечения составляет около двух недель, а вероятность появления побочных эффектов не должна превышать 15%. Большая часть из них - несерьезные, то есть не нужно из-за них прерывать назначенный гастроэнтерологом курс препаратов.
Схемы лечения
Схема терапии в первую очередь должна обеспечивать постоянный высокий уровень эрадикации бактерии. Схема эрадикации хеликобактер пилори подбирается в индивидуальном порядке в зависимости от чувствительности бактерии и реакции организма на препарат.
Схем эрадикации (ликвидации) много, и со временем их количество увеличивается. При этом все они направлены на достижение ряда задач, среди которых:
Разработка схем
На данный момент существенных результатов по всем перечисленным выше направлениям удалось добиться благодаря коллаборации ученых и фармацевтических предприятий. Еще в конце прошлого века была создана группа из наиболее влиятельных специалистов отрасли, усилия которой направлены на обмен знаниями об эрадикации.
Это позволило произвести прорыв в разработке методов лечения и осуществить более эффективные испытания. Наибольшего прогресса удалось добиться на конференции в Маастрихте в 1996 году. В честь этого события впоследствии и называли комплексы по лечению хеликобактер пилори.
- амоксициллин (0.5 г 4 раза в день или 1 г - 2 раза);
- кларитромицин, или джозамицин, или нифурател (стандартные дозы);
- висмута трикалия дицитрат (240 мг дважды в сутки или вдвое меньшая доза - четыре раза).
Указанная выше схема используется лишь для пациентов с атрофией слизистой оболочки желудка.
Четвертый вариант (для пожилых больных):
- стандартная дозировка ингибиторов;
- висмута трикалия дицитрат;
Четвертый вариант (альтернативный) состоит в приеме висмута трикалия дицитрата в стандартных дозировках на протяжении 28 дней с возможным краткосрочным задействованием ингибиторов.
Вторая линия
При отсутствии видимого эффекта применяется вторая линия эрадикации, позволяющая повысить эффективность процедуры.
Вариант первый:

Вариант второй:
- ингибиторы;
- висмута трикалия дицитрат;
- препараты нитрофурановой группы;
Вариант третий:
- ингибитор протонного насоса;
- висмута трикалия дицитрат (только 120 мг четырежды в сутки);
- рифаксимин (0.4 г дважды в сутки).
Третья линия
Существует также и третья линия, но ее распространение минимально из-за высокой эффективности перечисленных выше вариантов. Использование этой схемы имеет место лишь в тех случаях, когда показания не позволяют использовать первые две из-за аллергических реакций или неудовлетворительной реакции на лечение.
Хеликобактер пилори (лат. ) - спиралевидная грамотрицательная микроаэрофильная бактерия, инфицирующая слизистую оболочку желудка и двенадцатиперстной кишки . Иногда называют геликобактер пилори (см. Циммерман Я.С.).
Заблуждения, связанные с Helicobacter pylori
Нередко, при обнаружении , пациенты начинают беспокоиться об их эрадикации (уничтожении). Само наличие в желудочно-кишечном тракте не является причиной для немедленной терапии с применением антибиотиков или других средств. В России количество носителей достигает 70 % населения и подавляющее большинство из них не страдает какими-либо заболеваниями желудочно-кишечного тракта. Процедура эрадикации предполагает прием двух антибиотиков (например, кларитромицина и амоксициллина). У пациентов, имеющих повышенную чувствительность к антибиотикам, возможны аллергические реакции - от антибиотик-ассоциированной диареи (не тяжелое заболевание) до псевдомембранозного колита , вероятность возникновения которого мала, но процент летальных исходов большой. Кроме того, прием антибиотиков отрицательно воздействует на «дружественную» микрофлору кишечника , мочеполовых путей и способствует развитию резистентности к данному виду антибиотиков. Имеются данные, что после успешной эрадикации в течение ближайших лет чаще всего наблюдается реинфекция слизистой желудка, которая уже через 3 года составляет 32±11 %, через 5 лет - 82–87%, а через 7 лет - 90,9% (Циммерман Я.С.).Пока боль не проявилась, хеликобактериоз лечить не следует. Более того, у детей до восьмилетнего возраста вообще не рекомендуется проводить эрацикационную терапию, потому что у них иммунитет еще не сформирован, антитела к не вырабатываются. Если у них провести эрадикацию до 8-летнего возраста, то через день, пообщавшись кратковременно с другими детьми, «схватят» эти бактерии (П.Л. Щербаков).
Эрадикация может быть рекомендована для снижения риска развития рака желудка . Известно, что как минимум 90% случаев рака желука связаны с H. pylori-инфекцией (Старостин Б.Д.).
 |
 |
 |
| от экспериментально моноинфицированных мышей (A), слизистой оболочки желудка человека (B) и культивированные на пластине агара (C). Как выделенных от экспериментально инфицированных мышей, так и при биопсии человека поверхность является грубой, а жгутики имеют тенденцию склеиваться. За исключением коккоидной формы, морфология сравнительно хорошо сохраняется в культуре на агаре (С). Масштабные метки = 1 мкм. Источник: Stoffel M.H. et al. Distinction of Gastric Helicobacter spp. in Humans and Domestic Pets by Scanning Electron Microscopy / January 2001. DOI: 10.1046/j.1523-5378.2000.00036.x. Blackwell Science, 1083-4389/00/232–239. Inc. Volume 5 Number 4 2000. | ||
Факторы вирулентности Helicobacter pylori
Известно несколько факторов вирулентности, позволяющих заселять, а затем персистировать в организме хозяина (Скворцов В.В., Скворцова Е.М.).- Жгутики позволяют передвигаться в желудочном соке и слое слизи.
- способен прикрепляться к плазмолемме эпителиальных клеток желудка и разрушать компоненты цитоскелета этих клеток.
- вырабатывает уреазу и каталазу. Уреаза расщепляет мочевину, содержащуюся в желудочном соке, что повышает рН непосредственного окружения микроба и защищает его от бактерицидного действия кислой среды желудка.
- способен подавлять некоторые иммунные реакции, в частности фагоцитоз.
- вырабатывает адгезины, способствующие адгезии бактерий к эпителиальным клеткам и затрудняющие их фагоцитоз полиморфно-ядерными лейкоцитами.
Язва двенадцатиперстной кишки, ассоциированная с Helicobacter pylori
Основным местом обитания является слизистая оболочка антрального отдела желудка, пораженная воспалительно-атрофическим процессом - гастритом, ассоциированным с . Для развития язвы двенадцатиперстной кишки, ассоциированной с , необходимо наличие в слизистой оболочке двенадцатиперстной кишки участков желудочной метаплазии, которая в свою очередь связана с увеличение кислотности двенадцатиперстной кишки. Таким образом, язва двенадцатиперстной кишки, ассоциированная с и дуоденит всегда развиваются на фоне кислотно-пептической агрессии в двенадцатиперсную кишку, т.е. одновременно являются и кислотно-зависимой патологией. При этом важнейшим фактором гиперсекреции соляной кислоты в желудке является прямое влияние на секреторный процесс путем избыточного ощелачивания антрального отдела желудка продуктами гидролиза мочевины уреазой, вырабатываемой . Следствием избыточного ощелачивания является гипергастринемия, приводящая в свою очередь к гиперпродукции соляной кислоты. Нарушения в регуляции кислотообразования при ассоциированном с гастрите также обусловлены самим процессом специфического воспаления и его медиаторами (цитокинами и эпидермальными факторами роста), синтезируемыми в слизистой оболочке антрального отдела желудка в ответ на инфицирование , особенно выраженное у цитотоксичных штаммов. Данные штаммы могут не только вызывать выраженное воспаление в желудке, но и способствовать развитию деструктивных процессов – язвообразованию, в том числе в двенадцатиперстной кишки в участках желудочной метаплазии. Этому способствуют агрессивные факторы дуоденальной среды, снижение защитных свойств слизистого барьера, нарушение микроциркуляции (в том числе из-за ), наследственная предрасположенность. Все эти процессы приводят к появлению язвы (Маев И.В, Самсонов А.А.).
ощелачивания является гипергастринемия, приводящая в свою очередь к гиперпродукции соляной кислоты. Нарушения в регуляции кислотообразования при ассоциированном с гастрите также обусловлены самим процессом специфического воспаления и его медиаторами (цитокинами и эпидермальными факторами роста), синтезируемыми в слизистой оболочке антрального отдела желудка в ответ на инфицирование , особенно выраженное у цитотоксичных штаммов. Данные штаммы могут не только вызывать выраженное воспаление в желудке, но и способствовать развитию деструктивных процессов – язвообразованию, в том числе в двенадцатиперстной кишки в участках желудочной метаплазии. Этому способствуют агрессивные факторы дуоденальной среды, снижение защитных свойств слизистого барьера, нарушение микроциркуляции (в том числе из-за ), наследственная предрасположенность. Все эти процессы приводят к появлению язвы (Маев И.В, Самсонов А.А.).
Схемы эрадикации Helicobacter pylori
Всемирной организаций здравоохранения к активным препаратам в отношении отнесены метронидазол , тинидазол , коллоидный субцитрат висмута , кларитромицин , амоксициллин и тетрациклин (Подгорбунских Е.И., Маев И.В., Исаков В.А.).
Эрадикация не всегда достигает цели. Очень широкое и неправильное применение распространенных антибактериальных средств привело к повышению устойчивости к ним . На рисунке справа (взято из статьи Белоусовой Ю.Б., Карпова О.И., Белоусова Д.Ю. и Бекетова А.С.) показана динамика резистентности к метронидазолу, кларитромицину и амоксициллину штаммов , выделенных от взрослых (сверху) и от детей (снизу). Признано, что в разных странах мира (разных регионах) целесообразно применение разных схем. Ниже даны рекомендации по эрадикации , изложенные в Стандартах диагностики и лечения кислотозависимых и ассоциированных с Helicobacter pylori заболеваний принятых Научным обществом гастроэнтерологов России в 2010 г. Выбор схемы эрадикации зависит от наличия индивидуальной непереносимости пациентами конкретных лекарств, а также чувствительности штаммов к этим лекарствам. Применение кларитромицина в эрадикационных схемах возможно лишь в регионах, где резистентность к нему менее 15–20 %. В регионах с резистентностью выше 20 % его использование целесообразно только после определения чувствительности к кларитромицину бактериологическим методом или методом полимеразной цепной реакции.

В России отсутствуют полномасштабные исследования, устанавливающие уровень распространённости резистентнных к кларитромицину штаммов H. pylori . Однако имеется несколько локальных исследований, в каждом из которых установлен в терминологии Маастрихта IV низкий уровень резистентности и, исходя из этого, в российских условиях, скорее всего, более целесообразно применять левую часть схемы, обозначенную зелёным.
Профессиональные медицинские публикации, касающиеся заболеваний, ассоциированных с Helicobacter pylori
- Ивашкин В.Т., Маев И.В., Лапина Т.Л. и др. Клинические рекомендации Российской гастроэнтерологической ассоциации по диагностике и лечению инфекции Helicobacter pylori у взрослых // РЖГГК. 2018. № 28(1). С. 55–77 .
- Ивашкин В.Т., Маев И.В., Лапина Т.Л., Шептулин А.А., Трухманов А.С., Абдулхаков Р.А. и др. Лечение инфекции Helicobacter pylori: мейнстрим и новации // Рос журн гастроэнтерол гепатол колопроктол. 2017. № 27(4). С. 4-21 .
- Стандарты диагностики и лечения кислотозависимых и ассоциированных с Helicobacter pylori заболеваний (пятое Московское соглашение) // XIII съезд НОГР. 12 марта 2013 г.
- Стандарты диагностики и лечения кислотозависимых и ассоциированных с Helicobacter pylori заболеваний (четвертое Московское соглашение) / Методические рекомендации № 37 Департамента здравоохранения города Москвы. – М.: ЦНИИГ, 2010. – 12 с.
- Циммерман Я. С. Язвенная болезнь: критический анализ современного состояния проблемы // Экспериментальная и клиническая гастроэнтерология. - 2018. - 149(1). С. 80–89.
- Корниенко Е.А., Паролова Н.И. Антибиотикорезистентность Helicobacter pylori у детей и выбор терапии // Вопросы современной педиатрии. – 2006. – Том 5. – № 5. – с. 46–50.
- Циммерман Я.С. Проблема растущей резистентности микроорганизмов к антибактериальной терапии и перспективы эрадикации Helicobacter pylori-инфекции / В кн.: Нерешенные и спорные проблемы современной гастроэнтерологии. – М.: МЕДпресс-информ, 2013. С.147-166 .
- Диагностика и лечение инфекции Helicobacter pylori – отчет согласительной конференции Маастрихт IV / Флоренция // Вестник практического врача. Спецвыпуск 1. 2012. С. 6-22 .
- Исаков В.А. Диагностика и лечение инфекции, вызванной Helicobacter pylori: IV Маастрихтское соглашение / Новые рекомендации по диагностике и лечению инфекции H.Pylori – Маастрихт IV (Флоренция). Best Clinical Practice. Русское издание. 2012. Вып.2. С.4-23 .
- Маев И.В., Самсонов А.А., Андреев Д.Н., Кочетов С.А., Андреев Н.Г., Дичева Д.Т. Современные аспекты диагностики и лечения инфекции Helicobacter pylori // Медицинский Совет. 2012. №8. C. 10–19 .
- Ракитин Б.В. Информация о согласительной конференции по диагностике и лечению инфекции Helicobacter pylori «Маастрихт V» из доклада М. Лея на 42-ой научной сессии ЦНИИГ, 2-3 марта 2016 .
- Маев И.В., Рапопорт С.И., Гречушников В.Б., Самсонов А.А., Сакович Л.В., Афонин Б.В., Айвазова Р.А. Диагностическая значимость дыхательных тестов в диагностике инфекции Helicobacter pylori // Клиническая медицина. 2013. № 2. С. 29–33 .
- Казюлин А.Н., Парцваниа-Виноградова Е.В., Дичева Д.Т. и др. Оптимизация антихеликобактерной терапии в современной клинической практике // Consilium medicum. – 2016. - №8. – Том 18. С. 32-36 .
- Malfertheiner P, Megraud F, Morain CAO, Gisbert JP, Kuipers EJ, Axon AT, Bazzoli F, Gasbarrini A et al. Management of Helicobacter pylori infection-the Maastricht V/Florence Consensus Report // Gut 2016;0:1–25. doi:10.1136/gutjnl-2016-312288 .
- Старостин Б.Д. Лечение Helicobacter руlогі-инфекции - Маастрихсткий V/Флорентийский консенсусный отчет (перевод с комментариями) // Гастроэнтерология Санкт-Петербурга. 2017; (1): 2-22 .
- Маев И.В., Андреев Д.Н., Дичева Д.Т. и др. Диагностика и лечение инфекции Helicobacter pillory. Положения консенсуса Маастрихт V (2015 г.) // Архивъ внутренней медицины. Клинические рекомендации. - № 2. - 2017. С. 85-94 .
- Оганезова И.А., Авалуева Е.Б. Helicobacter pylori-негативная язвенная болезнь: исторические факты и современные реалии. Фарматека. 2017; Гастроэнтерология/Гепатология:16-20 .
Проведение эрадикации Helicobacter pylori у беременных и кормящих матерей
Эрадикация Helicobacter рylori согласно Маастрихтским консенсусам II-2000 и III-2005 у беременных не проводится. Решение вопроса о проведении эрадикации Helicobacter рylori ставится после родоразрешения и окончания периода кормления грудью (Ребров Б.А., Комарова Е.Б.).Распространённость Helicobacter pylori в разных странах и в России
По данным Всемирной гастроэнтерологической организации ( в развивающихся странах, 2010, WGO) более половины населения Земли является носителями ), при этом частота инфицированности значительно варьируется между различными странами, а также внутри этих стран. В целом, инфицированность возрастает с возрастом. В развивающихся странах инфицированность значительно более выражена у лиц молодого возраста, чем в развитых странах. ВГО приводит следующие цифры:
| Страна (регион) | Возрастные группы | Частота инфицированности |
| Европа | ||
| Восточная Европа | взрослые | 70 % |
| Западная Европа | взрослые | 30-50 % |
| Албания | 16-64 | 70,7 % |
| Болгария | 1-17 | 61,7 % |
| Чехия | 5-100 | 42,1 % |
| Эстония | 25-50 | 69 % |
| Германия | 50-74 | 48,8 % |
| Исландия | 25-50 | 36 % |
| Нидерланды | 2-4 | 1,2 % |
| Сербия | 7-18 | 36,4 % |
| Швеция | 25-50 | 11 % |
|
Северная Америка
|
||
| Канада | 5-18 | 7,1 % |
| Канада | 50-80 | 23,1 % |
| США и Канада | взрослые | 30 % |
|
Азия
|
||
| Сибирь | 5 | 30 % |
| Сибирь | 15-20 | 63 % |
| Сибирь | взрослые | 85 % |
| Бангладеш | взрослые | > 90 % |
| Индия | 0-4 | 22 % |
| Индия | 10-19 | 87 % |
| Индия | взрослые | 88 % |
| Япония | взрослые | 55-70 % |
|
Австралия и Океания
|
||
| Австралия | взрослые | 20 % |
Причиной разной инфицированности может быть социоэкономическое различие между популяциями. Заражение в основном происходит орально-оральным или фекально-оральным путями. Отсутствие санитарии, безопасной питьевой воды, базовых понятий о гигиене, а также ограниченная диета и большое скопление населения, могут играть роль в высокой распространенности инфекции.
Россия относится к странам с очень высокой распространенностью хеликобактерной инфекции. В некоторых регионах, например, в Восточной Сибири, эта цифра превышает 90% и в монголоидной, и в европеоидной популяции. В Москве инфицированность ниже. По данным ЦНИИ Гастроэнтерологии около 60% жителей ВАО Москвы – носители хеликобактера. Хотя в отдельных группах населения хеликобактер более распространен. В частности, среди работников промышленных предприятий Москвы инфицированы 88 % (
Эффективность лечения желудочно-кишечного тракта больного зависит от эрадикационного процесса в его организме. Бактерия хеликобактер пилори способна развивать осложнения заболеваний и патологию органов пищеварительной системы, поэтому необходимо определить индивидуальный подход для их уничтожения. Эрадикация бактерий является одним из самых важных этапов в лечении пациента.
Суть эрадикации заключается в применении стандартных и индивидуальных режимов лечения больного от бактерии хеликобактер пилори, которые направлены на полное ее уничтожение в организме. Уничтожение вредоносных микроорганизмов, осевших на слизистой оболочке желудка или двенадцатиперстной кишки, создает благоприятные условия для восстановления тканей, заживления эрозийных образований и язв, а также других повреждений.
Эрадикация бактерии хеликобактер пилори рассчитана на исключение обострения заболеваний, а также их повторного возникновения в реабилитационный период, когда организм больного изнурен длительным курсом лечения.
Схемы эрадикации вредоносных микроорганизмов в среднем предполагают терапию, рассчитанную на срок не более 14 дней. Данный лечебный процесс обладает достаточно низкой токсичностью. Эффективность применения медикаментозных препаратов и антибиотиков, которые назначает врач, выражается в достаточно высокой результативности. Около 90% пациентов после прохождения повторной диагностики желудочно-кишечного тракта считаются здоровыми, так как признаки хеликобактериоза отсутствуют.

Эрадикация бактерии хеликобактер пилори включает в себя некоторые особенности, которые делают данный процесс более универсальным в лечении больного. Одна из самых важных особенностей нацелена на повышение удобства следования такому курсу лечения.
Применение сильнодействующих ингибиторов протонной помпы помогают работе организма, а больному не обязательно следовать строгой диете. Конечно, питание должно быть сбалансированным и многие продукты должны быть исключены из рациона. Однако такая группа препаратов позволяет расширить круг продуктов, которые можно употреблять в период лечения.
Также курс продолжительности лечения может быть изменен при определенных условиях. Если у пациента улучшается самочувствие достаточно быстро, тогда 14 дневная терапия антибиотиками может замениться на 10 дневную или недельную.
Использование медикаментозных препаратов с комбинированными свойствами позволяет одновременно употреблять меньшее их количество.
Очень частое ежедневное употребление различных по своим свойствам лекарств может ухудшить состояние больного или нейтрализовать действие другого. Уменьшение числа принимаемых средств позволяет снизить вероятность причинить вред пациенту, а также не допустить высокого содержания химических соединений в крови. Также может быть изменена частота приема препаратов и их дозировка. Средства пролонгированной формы могут употребляться в меньшем количестве, но в таком случае курс лечения может быть рассчитан на более длительный период.

Эрадикация бактерии хеликобактер пилори позволяет предупредить ряд возможных побочных эффектов, которые могут проявиться в процессе лечения определенной схемой. Правильный и индивидуальный подбор медикаментозных препаратов, антибиотиков, ингибиторов протонной помпы, блокаторов Н2-гистаминовых рецепторов позволяет снизить вероятность непринятия организмом веществ, которые находятся в их составе . Также большое разнообразие препаратов повышает эффективность курса лечения.
Эрадикация опасных микроорганизмов хеликобактер пилори, начатая на раннем этапе её развития, позволяет преодолеть ее устойчивость к некоторым антибиотикам. Чем дольше бактерия продуцируется в клетках органов пищеварительной системы, тем большей устойчивостью она обладает. Данный вид микроорганизмов стойко переносит кислую среду желудка, а во время лечения малыми дозами антибиотиков сможет развить частичную устойчивость против них.
Подход в лечении может быть гибким. Если у больного наблюдается индивидуальная непереносимость отдельных компонентов в стандартной схеме, тогда некоторые из них могут быть заменены на аналогичные по своим свойствам лекарства.
Все эти характеристики позволяют увеличить эффективной эрадикции хеликобактер пилори и подобрать индивидуальный подход в лечении пациента.

Эрадикационная терапия должна отвечать основным требованиям лечебного курса:
- высокая результативность лечения препаратами;
- эффективное уничтожение вредоносных бактерий в организме;
- низкая частота возможных побочных эффектов у пациента;
- экономичность;
- активное влияние на язвенные процессы в желудочно-кишечном тракте и воздействие на поврежденные участки;
- низкий уровень влияния большинства резистентных штаммов на частоту эрадикационного процесса.
Чем лучше эти показатели при определенной схеме лечения, тем эффективней будет проходить процесс эрадикации бактерии хеликобактер пилори.
Эрадикационная терапия не всегда может оказать абсолютный результат. До сегодняшнего дня в медицине произошло много открытий и подходы в лечении также изменились.
Эффективность терапии возросла, однако все еще не может гарантировать полное выздоровление от вредоносных бактерий. Теперь эрадикация медикаментозными методами разделена на 3 уровня терапии. Каждая последующая схема подразумевает увеличение используемых взаимодополняющих препаратов разного действия и антибиотиков.

Показания к проведению эрадикационной терапии против хеликобактер пилори.
В первую очередь терапия нужна при полученных положительных результатах диагностики организма пациента на хеликобактериоз. Если данный вид бактерий стал причиной образования язвенной патологии желудка, лимфомы, разных форм гастрита.
Терапия может быть назначена, если обнаружены признаки раковой опухоли после резекции желудка. А также по желанию самого пациента, если его ближайшие родственники были больны на рак желудка, и только после детальной консультации врача.
Целесообразность проводить эрадикационную терапию хеликобактер пилори заключается в нескольких аспектах.
Функциональная диспепсия. Диспепсия во время эрадикации является оправданным выбором для профилактики в процессе лечения, которая способствует улучшению самочувствия пациента на значительный период времени (или до полного выздоровления).

Гастроэзофагеальная рефлюксия. Если лечение направлено на подавление выработки пищеварительной системой соляной кислоты и едких ферментов, а процесс эрадикационной терапии не связан с проявлением в организме существующей гастроэзофагеальной рефлюксной болезни.
Поражение гастродуоденальной слизистой оболочки органов пищеварения. Если поражения индуцированы во время приема нестероидных противовоспалительных средств, тогда необходима эрадикационная терапия. Это связано с тем, что применение нестероидных противовоспалительных препаратов не может в достаточной мере предотвратить рецидивы кровотечения при язвенной патологии у больного. Также такие препараты не ускоряют процесс восстановления желудочной и дуоденальной язвы, они помогают облегчить симптомы заболевания, но не устранить причину их появления.
Видео “Helicobacter Pylori”
Схемы и препараты
Наличие показаний к проведению эрадикации бактерий хеликобактер пилори определяется после диагностики пациента.
Если в желудочно-кишечном тракте больного обнаружены признаки присутствия вредоносных микроорганизмов или же ДНК этих бактерий, тогда врачу необходимо поставить правильный диагноз и назначить схему лечения пациента.
Так как хеликобактер пилори присутствует в организмах большей части населения планеты, она не всегда находится на стадии активного развития. Если у человека не наблюдаются обострения симптомов заболевания пищеварительной системы, тогда не стоит предпринимать поспешного лечения антибиотическими препаратами.
Проведение диагностики разными методами позволяет с высокой точностью установить наличие бактерий в организме, стадию их развития и поражения желудка или двенадцатиперстной кишки. Но лишь присутствие хеликобактер пилори в пищеварительных органах не достаточный повод для начала эрадикации возбудителя.

Иногда присутствие бактерии выявляется случайным образом во время проведения анализов биологического материала на наличие возбудителей других заболеваний.
Без характерных признаков заболевания желудочно-кишечного тракта лечение хеликобактериоза проходит по консервативной методике.
Такая схема определяется гастроэнтерологом. Врач назначает особый режим питания и диеты. Соблюдения ряда профилактических мер помогут предотвратить распространение бактерий в желудке и кишечнике. В такой ситуации терапия с применением антибиотиков и других медикаментозных препаратов не считается оправданной. Во время профилактики пищеварительной системы радикальные схемы лечения могут нанести больший вред человеку, чем следование консервативным методам.
При отсутствии симптомов хеликобактериоза, кроме режима питания и диеты, определяется схема применения профилактических средств. Они основаны на натуральных природных компонентах, а не на фармакологических препаратах.
В качестве консервативной терапии используются отвары на основе лекарственных трав, употребление меда и прополиса, приготовление различных настоек и чая.

Если же проведение диагностики пациента проводилось целенаправленно по причине его беспокойства рядом определенных симптомов, тогда вероятность обнаружить присутствующую бактерию в организме очень высока. Также проведение анализов необходимо при наличии некоторых других показаний к эрадикации хеликобактер пилори.
Комплексный подход в диагностике и исследовании биологического материала больного позволяет определить врачу схему лечения.
Методика лечения подбивается в индивидуальном порядке с учетом всех показаний, полученных результатов анализа и особенностей организма пациента.
Эрадикация хеликобактериоза подразумевает активное лечение с применением антибиотиков во всех схемах терапии.
Схема терапии первой линии. Лечение по такой методике используется значительно чаще, чем другие комбинации препаратов. Курс лечения первой линии направлен на одновременное использование определенного вида антибиотиков и дополняющего его препарата.

Дозировка антибиотиками определяется лечащим врачом в индивидуальном порядке с учетом всех важных показателей (вес, возраст и другие).
Так во время эрадикации хеликобактер пилори могут быть использованы антибиотики в разном сочетании.
1 метод. Обычно назначается при диагностике атрофии слизистой оболочки желудочно-кишечного тракта. Антибиотики в стандартной дозировке для взрослого человека.
Амоксициклин – по 500 мг на 4 приема в течение дня или по 1 грамму на 2 приема утром и вечером.
Кларитромицин – по 500 мг 2 раза в сутки.
Джозамицин – по 1 грамму 2 раза в сутки.
Нифуратель – по 400 мг 2 раза в сутки.
Антибиотики должны применяться с взаимодополняющим препаратом. В данном методе чаще всего используется ингибитор протонной помпы.
Омепразол – по 20 мг. Лансопразол – по 30 мг. Пантопразол – по 40 мг. Эзомепразол – по 20 мг. Рабепразол – по 20 мг. Употребляется 2 раза в сутки.
2 метод. Медикаментозные препараты, которые используются в первой методике, также могут назначаться с добавлением дополнительного компонента – висмута трикалия дицитрата – по 120 мг 4 раза в сутки или удвоенная дозировка 2 раза в сутки.
Эрадикация по схеме первой линии обычно проходит в течение 2 недель. Возможно сокращение срока.

Схема терапии второй линии. Гастроэнтеролог назначает такую терапию в том случае, если предыдущий подход не дал необходимых результатов.
Данная методика заключается в применении одновременно одного антибиотика и двух взаимодополняющих препаратов.
Одно средство относится к группе ингибиторов протонной помпы, а другое к группе блокаторов Н2-гистаминовых рецепторов.
Также для эрадикации хеликобактериоза второй линии могут использоваться антибиотики Тетрациклин и Метронидазол – по 500 мг 3 раза в сутки.
Среди ингибиторов протонной помпы врач выбирает наиболее подходящий препарат: Маалокс, Фосфалюгель или Альмагель.
К блокаторам Н2-гистаминовых рецепторов относятся Ранитидин, Квамател, Роксатидин и Фамотидин. Один из них в обязательном порядке должен быть включен в схему лечения.

Каждый метод лечения может иметь разную дозировку антибиотиков и их комбинирование с другими препаратами.
Использование одновременно таких трех групп препаратов позволяет увеличить эффективность процесса эрадикации. Лечение по данной схеме рассчитано на 10 дней.
Схема комбинированной терапии. Назначается в том случае, если больному не помогла тритерапия хеликобактериоза.
Данная схема подразумевает максимально возможное использование медикаментов (с учетом передозировки). Назначается два вида антибиотиков и также дополняющие препараты.
Одновременно могут комбинироваться все виды антибиотиков. Например, Тетрациклин и Метронидазол, Кларитромицин и Амоксициклин, и другие сочетания.
Правильный подбор сочетания антибиотиков снизит вероятность конфликта веществ, входящих в их состав, также будет способствовать расширению спектра их действия.
Употребление большего количества медикаментов снижает курс терапии до 7 дней.